乳幼児(生後6か月~5歳)の接種にはどのような副反応がありますか。
- 安全性は既承認の製剤と同様であり、接種部位の痛みや疲労、発熱、頭痛等、様々な症状が確認されていますが、ほとんどが軽度または中等度であり回復していることなど、現時点で得られている情報からは、安全性に重大な懸念は認められていないと判断されています。
令和5年(2023年)11月1日現在、ファイザー社のオミクロン株対応1価ワクチン(XBB.1.5)による生後6か月~4歳を対象とした初回接種と追加接種、及びモデルナ社のオミクロン株対応1価ワクチン(XBB.1.5)による生後6か月~5歳を対象とした初回接種の使用が可能となっています。その安全性については、従来型1価ワクチン(従来株)とオミクロン株対応2価ワクチン(従来株/BA.1又はBA.4-5)の安全性について、これまで実施された臨床試験におけるデータや接種後の副反応の発現状況等から、大きな差が無いことが確認されていることを踏まえ、既承認の製剤と基本的には同様であり、特段の懸念はないものと考えられ、それぞれ令和5年9月1日及び同年10月24日に薬事承認されています。
また、既承認の製剤であるファイザー社及びモデルナ社の従来型1価ワクチン(従来株)とオミクロン株対応2価ワクチン(従来株/BA.1又はBA.4-5)については、主な副反応として、注射した部分の痛み、頭痛、疲労、発熱等がありますが、現時点で重大な懸念は認められないことが薬事承認審査で確認されています。
<参考>
ファイザー社のワクチン(1価、従来株)は、生後6か月~4歳の接種において、接種部位の痛みや疲労、発熱、頭痛等、様々な症状が臨床試験で確認されていますが、ほとんどが軽度または中等度であり回復していることや、実薬群とプラセボ(生理食塩水)群とで大きな差はなかったこと等、現時点で得られている情報から、安全性に重大な懸念は認められていないと判断されています。
生後6~23か月の被験者において、注射部位の圧痛は接種当日(中央値)に発現し、持続期間は1 日(中央値)であり、その他の全身反応は接種翌日~4.5 日(中央値)に発現し、持続期間は1~2 日(中央値)と報告されています。また、2~4歳の被験者において、注射部位の疼痛は接種当日(中央値)に発現し、持続期間は1日(中央値)であり、その他の全身反応は接種翌日~5日(中央値)に発現し、持続期間は1~2.5日(中央値)と報告されています。
他の年代とは異なり、自ら症状を訴えることができない生後6か月~1歳では易刺激性(機嫌が悪い)や食欲減退、傾眠傾向等が報告されていますが、プラセボ(生理食塩水)群とは大きな差がなかったと報告されています。
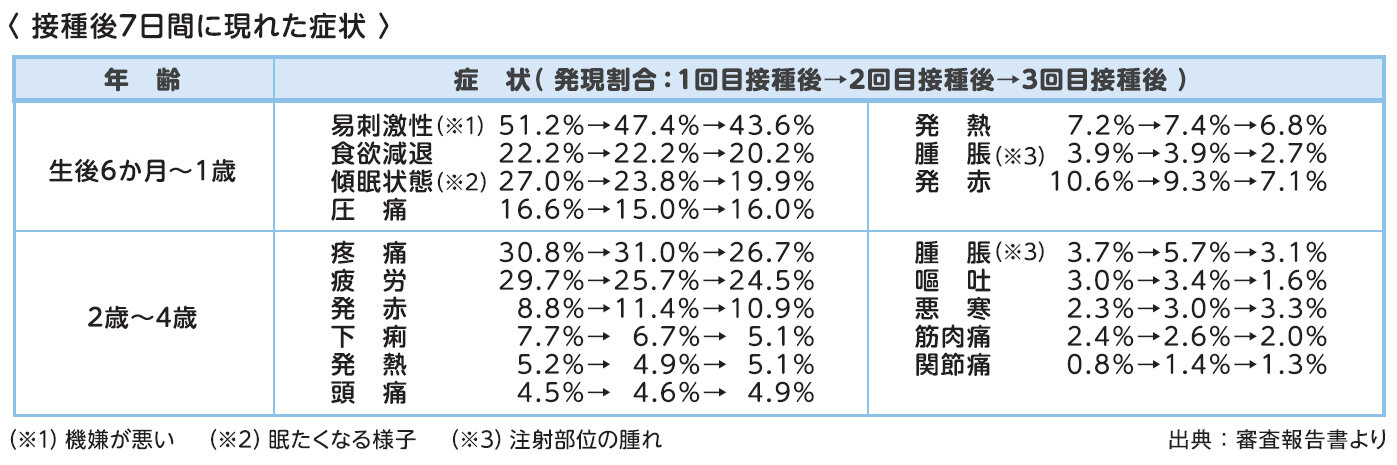
※厚生労働省リーフレット「新型コロナワクチン接種についてのお知らせ(生後6か月~4歳のお子様の保護者の方へ)」より抜粋
厚生労働省では、接種後の副反応を疑う事例を収集し、専門家による評価を行うとともに、接種後の健康状況に係る調査を実施しています。
同調査の令和5年10月27日の中間報告によれば、ファイザー社ワクチン(6か月~4歳用)の接種によるスパイクタンパク質(従来株)に対する幾何平均抗体価について、接種前では14U/mL、初回接種後(3回で1セット)1か月後では9,977U/mL、3か月後では3,975U/mLでした。安全性については、1~3回目接種後、一部の方に発熱や局所の疼痛等がみられました。接種後の体温変化を時系列で検討したところ、接種数日後にみられた偶発的な発熱、乳児期に感染しやすい感染症に罹患した事例など、ワクチン接種とは直接関係しない事象が発熱の発現率に影響している可能性があるとされています。今後も新たな知見が得られ次第、速やかにお知らせしていきます。
(参考資料)
新変異株対応のコロナワクチンの評価方針について(薬事・食品衛生審議会医薬品第二部会資料)
ファイザー社のオミクロン株対応1価ワクチン(XBB.1.5)の審査結果
ファイザー社ワクチンの添付文書(PMDAのHP)
PMDAの審査報告書(モデルナ社のオミクロン株対応1価ワクチン(初回免疫))
モデルナ社ワクチンの添付文書(PMDAのHP)
PMDAの審査報告書(ファイザー社のワクチン(生後6か月~4歳用))
乳幼児(生後6か月~4歳)に対する新型コロナワクチンの有効性、安全性等(第38回厚生科学審議会予防接種・ワクチン分科会資料より抜粋)
新型コロナワクチンの初回接種後の健康状況調査
検索
新型コロナワクチン
コールセンター
- 対応言語
- 日本語・英語・中国語・韓国語
ポルトガル語・スペイン語・タイ語・ベトナム語 - 受付時間(土日・祝日も実施) ※日本時間
-
日本語・英語・中国語・韓国語・ポルトガル語・スペイン語 9時00分~21時00分 タイ語 9時00分~18時00分 ベトナム語 10時00分~19時00分

